Содержание
- 2. Более половины всех используемых в настоящее время в мире антибиотиков составляют бета-лактамы. Их объединяют в одну
- 3. Классы бета-лактамных антибиотиков Пенициллины (пенамы); Цефалоспорины (цефемы); Цефамицины; Оксацефемы; Пенемы; Монобактамы; Карбапенемы (тиенамицин); Клавуланаты; Нокардицины; Комбинированные
- 4. ЛАКТАМЫ
- 5. ЛАКТАМЫ - это циклические амиды, образующиеся при перегруппировке оксимов циклических кетонов, что сопровождается расширением цикла (аминокислоты
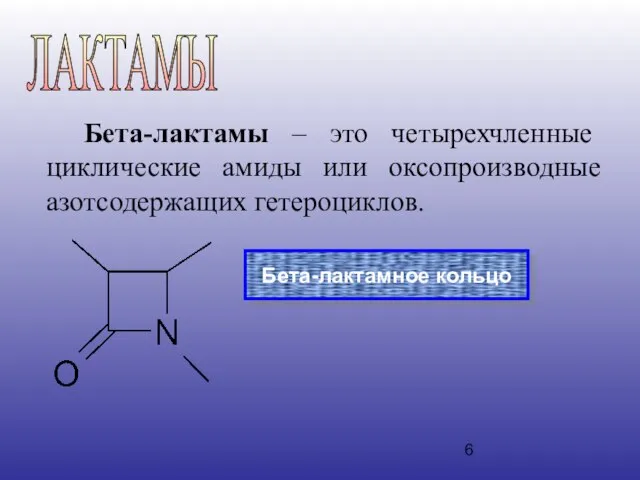
- 6. Бета-лактамы – это четырехчленные циклические амиды или оксопроизводные азотсодержащих гетероциклов. ЛАКТАМЫ Бета-лактамное кольцо
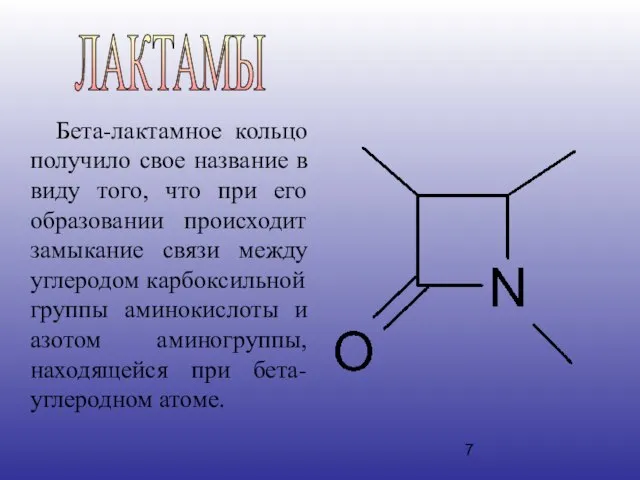
- 7. Бета-лактамное кольцо получило свое название в виду того, что при его образовании происходит замыкание связи между
- 9. Поиск и получение новых бета-лактамных антибиотиков осуществляется путем направленной модификации бета-лактамов, связанной с введением заместителей, изменяющих
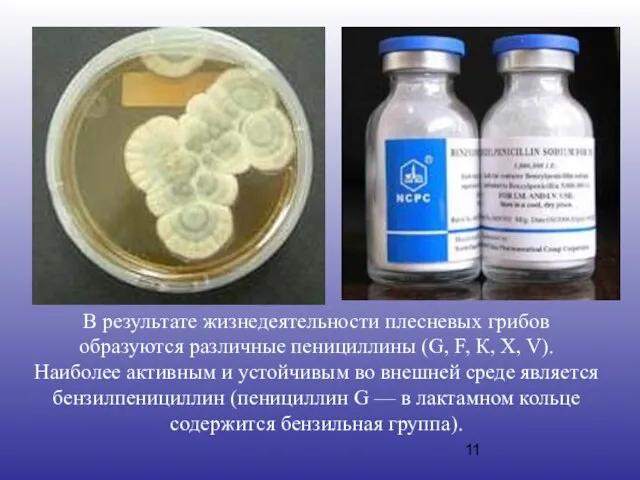
- 11. В результате жизнедеятельности плесневых грибов образуются различные пенициллины (G, F, К, X, V). Наиболее активным и
- 12. П Е Н И Ц И Л Л И Н Ы
- 13. I. Природные (биосинтетические): Короткого действия: бензилпенициллина натриевая соль (пенициллин); бензилпенициллина калиевая соль; феноксиметилпенициллин; Длительного действия: бензилпенициллинпрокаин
- 14. II. Полусинтетические: Изоксазоилпенициллины (антистафилококковые, резистентные к бета-лактамазам): оксациллин, клоксациллин, диклоксациллин; Аминопенициллины: ампициллин, амоксициллин; Карбоксипенициллины: карбенициллин, тикарциллин,
- 15. Биосинтетические Биосинтетические (природные) пенициллины получают из культуральной среды, на которой произрастают определенные штаммы плесневых грибов (Penicillium),
- 16. Полусинтетические Полусинтетические пенициллины создаются путем ферментативного гидролиза плесневых грибов с последующей химической модификацией 6-аминопенициллановой кислоты, являющейся
- 17. Действуют пенициллины бактерицидно, оказывая влияние только на делящиеся микроорганизмы. Антибактериальное действие связано с нарушением синтеза клеточной
- 18. Бактерицидное действие На делящиеся микроорганизмы Мишень действия – транспептидаза П Е Н И Ц И Л
- 19. Классификация полусинтетических пенициллинов
- 20. Пенициллин - природное вещество, продуцируемое разными видами плесневого гриба пенициллиума (Penicillium chrysogenum, notatum), а также стрептомицетами.
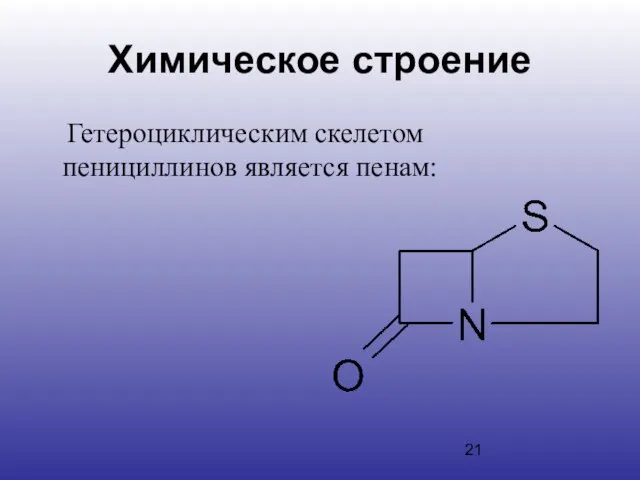
- 21. Химическое строение Гетероциклическим скелетом пенициллинов является пенам:
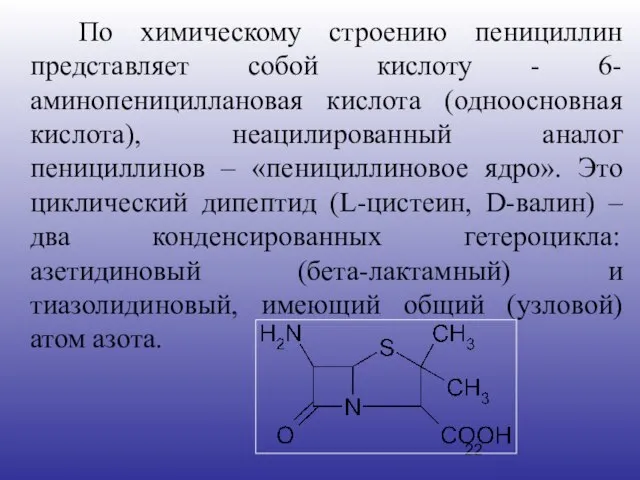
- 22. По химическому строению пенициллин представляет собой кислоту - 6-аминопенициллановая кислота (одноосновная кислота), неацилированный аналог пенициллинов –
- 23. Пенициллины (и все другие бета-лактамы) обладают бактерицидным эффектом в отношении микроорганизмов, находящихся в фазе роста. Бета-лактамные
- 24. Основным компонентом внешней мембраны у Pseudomonas aeruginosa, как и у других грамотрицательных микроорганизмов, является липополисахаридный слой,
- 25. Схематическое изображение инактивации антибиотиков в периплазматическом пространстве клеточной стенки грамотрицательной бактерии. 1. Тример поринового белка. 2.
- 26. Мишень действия пенициллинов – пенициллиносвязывающие белки (ПСБ) бактерий, выполняющие роль ферментов (транспептидаз и карбоксипептидаз) на завершающем
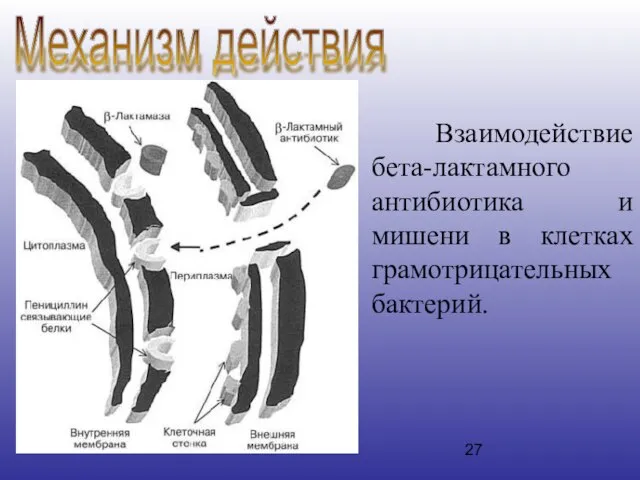
- 27. Взаимодействие бета-лактамного антибиотика и мишени в клетках грамотрицательных бактерий. Механизм действия
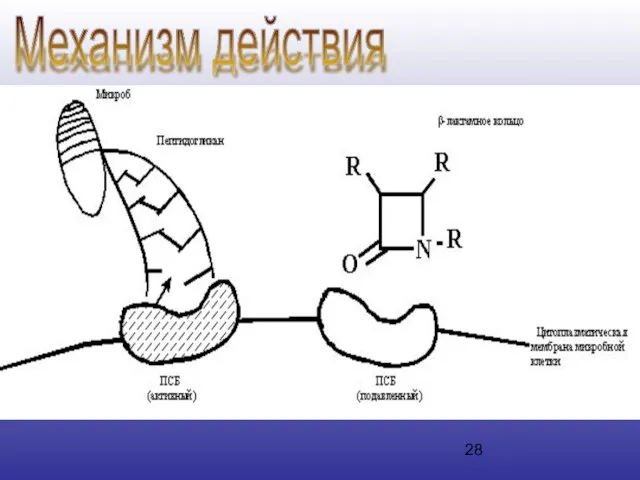
- 28. Механизм действия
- 29. Обязательным компонентом наружной мембраны прокариотических микроорганизмов (кроме микоплазм) является пептидогликан, представляющий собой биологический полимер, состоящий из
- 30. Блокирование синтеза ПСБ ведет к прекращению деления и последующей гибели бактерий. Связывание бета-лактамного антибиотика с ПСБ
- 31. Поскольку пептидогликан и ПСБ у человека отсутствуют, специфическая токсичность в отношении макроорганизма для бета-лактамов нехарактерна. Бактерицидная
- 32. Для преодоления широко распространенной среди микроорганизмов приобретенной устойчивости, связанной с продукцией особых ферментов – бета-лактамаз (расположены
- 33. Ингибиторы бета-лактамаз Тазобактам Сульбактам Клавуланат
- 34. У Гр(-) бактерий бета-лактамазы локализованы в периплазматическом пространстве, а у Гр(+) свободно диффундируют в окружающую бактерии
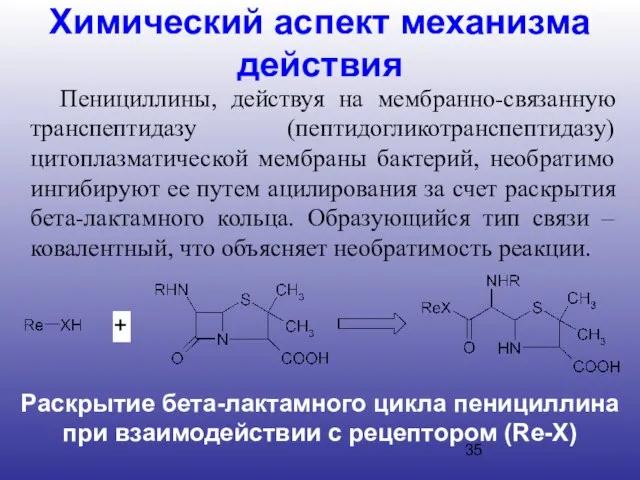
- 35. Химический аспект механизма действия Пенициллины, действуя на мембранно-связанную транспептидазу (пептидогликотранспептидазу) цитоплазматической мембраны бактерий, необратимо ингибируют ее
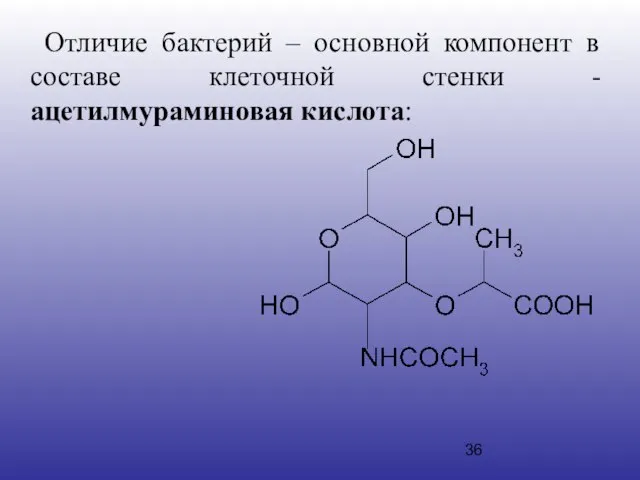
- 36. Отличие бактерий – основной компонент в составе клеточной стенки - ацетилмураминовая кислота:
- 37. Ацетилмураминовая кислота связывается с полипептидами на участках типа –CO-NH-CH(CH3)-CO-NH-CH(COR)-CH2-CH2-CO-NH-CH[(CH2)4NH2]-CO-. И действие пенициллинов основано на блокаде включения
- 38. Этот мономер – пептидогликан состоит из описанного выше муропептида, связанного с углеводными компонентами. Создание полимера протекает
- 39. Т.о., пенициллины являются антагонистами D-аланил-D-аланинов, причем необратимость их взаимодействия с транспептидазой обусловлена образованием прочной ковалентной связи.
- 40. Клеточная стенка у бактерий имеет жесткую структуру, она придает микроорганизмам форму и обеспечивает их защиту от
- 41. В процессе биосинтеза пептидогликана участвуют около 30 бактериальных ферментов, этот процесс состоит из 3 этапов. Считают,
- 42. Нерастущие, «покоящиеся» клетки не затрагиваются пенициллинами. С нарушением синтеза клеточной оболочки под действием пенициллина связано образование
- 43. Гидролизуют бета-лактамный цикл и инактивируют пенициллины (лишают способности выступать антибиотик в качестве ацилирующих агентов). Бета-лактамазный механизм
- 44. Бета-лактамазы расширенного спектра действия: Бактериальные ферменты, вырабатываемые микроорганизмами семейства Enterobacteriaceae (в основном K.pneumoniae, E.coli, реже другими
- 45. Бета-лактамазы широкого спектра действия: Бактериальные ферменты, вырабатываемые в основном представителями семейства Enterobacteriaceae и некоторыми неферментирующими бактериями,
- 46. К практически важным свойствам бета-лактамаз относятся: Субстратный профиль (способность к преимущественному гидролизу тех или иных БЛА,
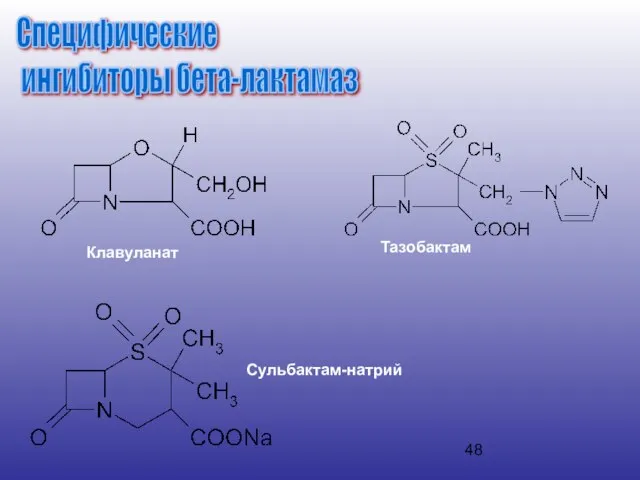
- 47. Специфические ингибиторы бета-лактамаз
- 48. Специфические ингибиторы бета-лактамаз Клавуланат Тазобактам Сульбактам-натрий
- 49. Данные вещества, подобно бета-лактамным антибиотикам, содержат лактамное кольцо. Они «захватываются» бета-лактамазами, вследствие чего происходит необратимое ингибирование
- 50. Сами ингибиторы бета-лактамаз обладают слабой антибактериальной активностью. Наиболее эффективным неконкурентным ингибитором бета-лактамаз различной этиологии является клавулановая
- 51. Биосинтетические пенициллины
- 52. Benzylpenicillinum-natrium, пенициллин G, или просто пенициллин. Форма выпуска Порошок для приготовления инъекционных растворов во флаконах по
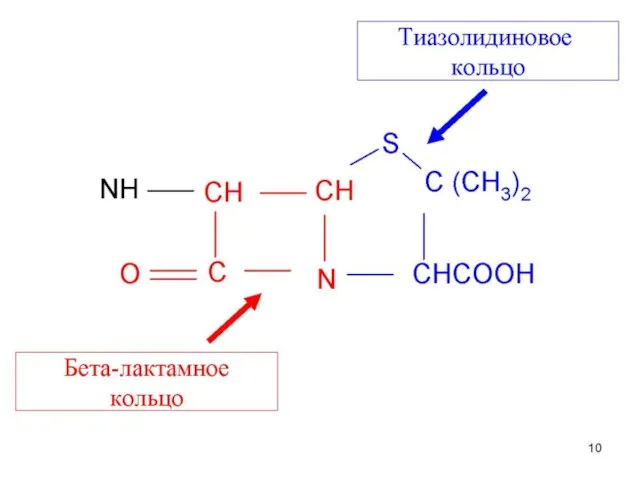
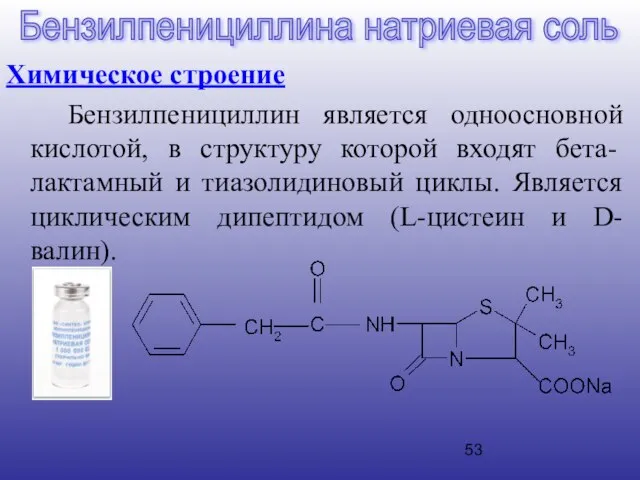
- 53. Химическое строение Бензилпенициллин является одноосновной кислотой, в структуру которой входят бета-лактамный и тиазолидиновый циклы. Является циклическим
- 54. Спектр антибактериальной активности Бензилпенициллина натриевая соль
- 55. Бета-лактамные антибиотики ШИРОКИЙ СПЕКТР АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТИ
- 56. Не действует на большинство грамотрицательных бактерий, риккетсии, вирусы, простейшие, грибы; штаммы стафилококков, продуцирующие бета-лактамазы; бактерии кишечной
- 57. Плохо абсорбируется в ЖКТ. Разрушается в кислой среде желудка и пенициллиназой, продуцируемой микрофлорой кишечника, поэтому применяется
- 58. При подкожных инъекциях скорость абсорбции непостоянна, Сmax в среднем через 60 мин. Через 3-4 часа после
- 59. При инфекциях, вызванных чувствительными к бензилпенициллину микроорганизмами (г.о. стрептококками, менингококками и пневмококками): пневмонии, остром и подостром
- 60. Бензилпенициллина натриевую соль вводят в виде растворов подкожно, внутримышечно, при необходимости – внутривенно или в полости
- 61. Внутримышечное введение бензилпенициллина является наиболее распространенным. Для внутримышечного введения препарат готовят ex tempore, добавляя к содержимому
- 63. Взрослым вводится по 2 000 000-12 000 000 ЕД в сутки (в 4-6 приемов); при менингите,
- 64. Реестр побочных эффектов Головная боль, повышение температуры тела, экзантема, боли в суставах, эозинофилия, ангионевротический отек, анафилактический
- 66. Скачать презентацию
























![Ацетилмураминовая кислота связывается с полипептидами на участках типа –CO-NH-CH(CH3)-CO-NH-CH(COR)-CH2-CH2-CO-NH-CH[(CH2)4NH2]-CO-. И действие пенициллинов](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/856188/slide-36.jpg)
























 Клиническая анатомия лобной пазухи, лобного кармана по данным рентгеновской компьютерной томографии
Клиническая анатомия лобной пазухи, лобного кармана по данным рентгеновской компьютерной томографии Определение понятий иридоиды и горечи
Определение понятий иридоиды и горечи Методы улучшения работы головного мозга
Методы улучшения работы головного мозга Гормоны, как лекарственные вещества. Анализ, применение и хранение. (Тема 4)
Гормоны, как лекарственные вещества. Анализ, применение и хранение. (Тема 4) Воздухоносные пути и легкие: строение и функции
Воздухоносные пути и легкие: строение и функции Структура ХНИЗ как составляющих приоритетных классов заболеваний
Структура ХНИЗ как составляющих приоритетных классов заболеваний Столбняк. Возбудитель
Столбняк. Возбудитель Меры безопасности при сильном морозе
Меры безопасности при сильном морозе Medical academy named after s.i georgievsky of vernadsky CFU
Medical academy named after s.i georgievsky of vernadsky CFU Заседание кружка ОХиТА
Заседание кружка ОХиТА Изотоник АкваНорм
Изотоник АкваНорм Витамины
Витамины Gonoreya (1)
Gonoreya (1) Сердечно-сосудистые заболевания
Сердечно-сосудистые заболевания Пространственные параметры жилища и их роль в обеспечении гигиенического комфорта проживания
Пространственные параметры жилища и их роль в обеспечении гигиенического комфорта проживания Лабораторное обследование больных с ОРВИ/гриппом
Лабораторное обследование больных с ОРВИ/гриппом Медицинская визуализация. Современные методы обследования человеческого организма
Медицинская визуализация. Современные методы обследования человеческого организма Опухоли. Тема 1
Опухоли. Тема 1 Влияние вредных привычек на внутриутробное развитие плода
Влияние вредных привычек на внутриутробное развитие плода Введение в нозологию
Введение в нозологию Общие осложнения при проведении местной анестезии
Общие осложнения при проведении местной анестезии Балалардағы ЭхоКГ жүргізу тәсілі және функциональды сынамалар
Балалардағы ЭхоКГ жүргізу тәсілі және функциональды сынамалар Термические поражения. Электротравма
Термические поражения. Электротравма Седативные препараты. Фаб концепция
Седативные препараты. Фаб концепция Зачетное занятие по медицине
Зачетное занятие по медицине Аритмии и блокады
Аритмии и блокады Уроки пандемии гриппа H1N1/09: год 2016
Уроки пандемии гриппа H1N1/09: год 2016 ДВС-синдром (диссеминированное внутрисосудистое свёртывание) в акушерской практике
ДВС-синдром (диссеминированное внутрисосудистое свёртывание) в акушерской практике