Содержание
- 2. Цель? Переливание компонентов крови должно производиться по строгим показаниям, когда требуемый лечебный эффект может быть достигнут
- 3. Гемотрансфузия осуществляется врачом, прошедшим обучение, сдавшим зачет и имеющим допуск к проведению гемотрансфузии.
- 4. Перед назначением гемотрансфузии (или при поступлении больного в стационар) собирают трансфузионный, а у женщин, кроме того,
- 5. У всех больных, которым может потребоваться переливание компонентов крови, должны быть проведены иммуногематологические исследования крови.
- 6. Для повышения иммуногематологической безопасности при использовании компонентов крови целесообразно разделить реципиентов на две группы: - «опасные
- 7. «Опасные реципиенты» 1. Больные с биологической особенностью образца крови (наличие слабых вариантов антигенов, парциальных антигенов, врожденный
- 8. 2. Больные с наличием аллоиммунных антиэритроцитарных антител любой активности и специфичности. 3. Больные с отягощенным акушерским
- 9. 4. Беременные женщины. 5. Дети. 6. Больные с онкогематологическими заболеваниями. 7. Больные с тяжелыми поражениями почек
- 10. 8. Больные, у которых выявлена несовместимость в любой из проб. 9. Больные, которым планируется перелить компоненты
- 11. Опасным реципиентам гемотрансфузии проводят только после индивидуального подбора компонентов крови
- 12. Алгоритм иммуногематологического исследования крови реципиентов 1. Первичное определение группы крови реципиента проводит лечащий (дежурный) врач. 2.
- 13. Объем исследования, проводимого лечащим (дежурным) врачом: - определение группы крови системы АВО простой реакцией изогемагглютинирующими сыворотками,
- 14. Результат первичного исследования лечащий врач записывает на этикетку, прикрепленную к пробирке с кровью реципиента, а также
- 15. Этикетка, прикрепленная к пробирке с кровью реципиента, должна содержать следующие данные: наименование лечебного отделения Ф. И.О.,
- 16. Объем обязательных исследований при подтверждающем определении: определение группы крови системы АВО перекрестной реакцией; определение антигена D
- 17. Результаты подтверждающего исследования регистрируют в специальном журнале, пронумерованном, прошнурованном, заверенном подписью главного врача и печатью, имеющем
- 18. Заключение о результатах подтверждающего исследования крови реципиента направляют в лечебное отделение. При совпадении результатов первичного и
- 19. При несовпадении результатов исследования специалист, выявивший несовпадение, НЕЗАМЕДЛИТЕЛЬНО сообщает лечащему врачу (устно и письменно), и комиссионно,
- 20. Если при подтверждающем иммуногематологическом исследовании выявлены: - аллоиммунные антиэритроцитарные антитела любой специфичности и активности; - фиксированные
- 21. Образец крови реципиента после подтверждающего иммуногематологического исследования хранится в лаборатории в течение 3 суток и в
- 22. Если при подтверждающем иммуногематологическом исследовании выявлены аллоиммунные антиэритроцитарные антитела любой специфичности и активности; фиксированные на эритроцитах
- 23. Если показания для гемотрансфузии являются абсолютными, то переливание проводят только после индивидуального подбора.
- 24. Показания к назначению СЗП При продолжающемся кровотечении, операции при показателях МНО>1,5, АЧТВ >45 сек
- 25. Lacroix J; N Eng J Med 2007; 356:1609-1619 Исследование TRIPICU. Протокол Либеральная стратегия Переливание при Hb
- 26. Lacroix J; N Eng J Med 2007; 356:1609-1619 Исследование TRIPICU. Заключение „… может безопасно сократить частоту
- 27. NEJM 2007;356:1609-1619 Lacroix J. et al
- 28. Эритроциты Планета Обедненные лейкоцитами Россия Фильтрованные
- 29. Остаточные лейкоциты ??? Фильтрованные Нужен метод и контроль качества
- 30. Приказ МЗ РФ № 193 от 7.05.2003 «О внедрении в практику работы службы крови в Российской
- 31. Методические рекомендации по лабораторному предупреждению передачи ВИЧ при переливании крови и ее компонентов (утв. Минздравсоцразвития России
- 32. ДИРЕКТИВА 2002/98/ЕС от 27.01.2003 Обследование должно проводится с применением последних достижений науки, которые отражают лучшую практику,
- 35. Вариабельны в зависимости от: Глубина анестезии Миорелаксация Температура тела FiO2 Функция миокарда ОЦК Замещение объема „Критические“
- 36. Соотношение перелитых доз эритроцитов : СЗП Финляндия 6,0 Германия 3,2 США 3,6 Швеция 3,7 Дания 5,8
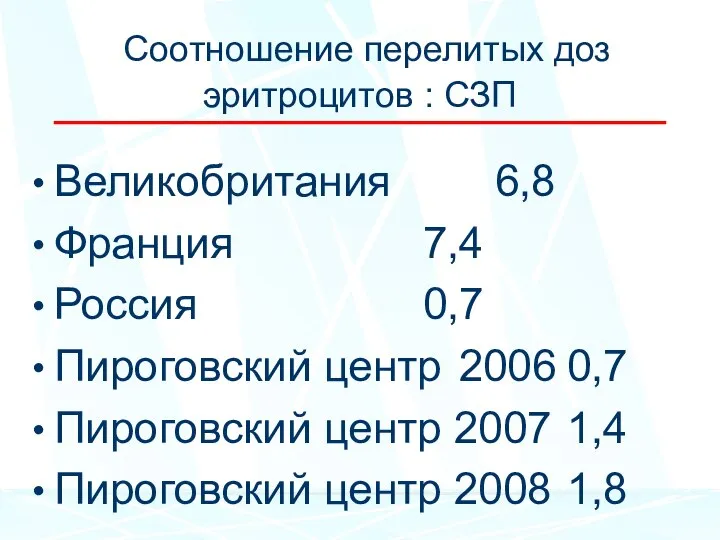
- 37. Соотношение перелитых доз эритроцитов : СЗП Великобритания 6,8 Франция 7,4 Россия 0,7 Пироговский центр 2006 0,7
- 38. Инструкция по применению компонентов крови (утв. приказом Минздрава России от 25 ноября 2002 г. № 363)
- 39. Seekamp A. Eur J Emerg Med 1995:2;28 Активность факторов свертывания: 37 оС 100% 37±3 оС 22
- 42. При трансфузиях новорожденным, эритроциты и плазму делили в четыре контейнера. Донорское воздействие сократилось на - 57%.
- 44. Скачать презентацию







































 Что такое COVID-19?
Что такое COVID-19? Сестринское обследование пациентов терапевтического профиля
Сестринское обследование пациентов терапевтического профиля Этическое и правовое регулирование научных исследований
Этическое и правовое регулирование научных исследований Общая эпидемиология
Общая эпидемиология Перелом предплечья
Перелом предплечья Варикозная болезнь
Варикозная болезнь Холера. Что такое холера?
Холера. Что такое холера? Қант диабетінің қауіп факторлары
Қант диабетінің қауіп факторлары Сосудистый шов
Сосудистый шов Первая медицинская помощь при переломах
Первая медицинская помощь при переломах Эпилепсия: причины, диагностика, лечение
Эпилепсия: причины, диагностика, лечение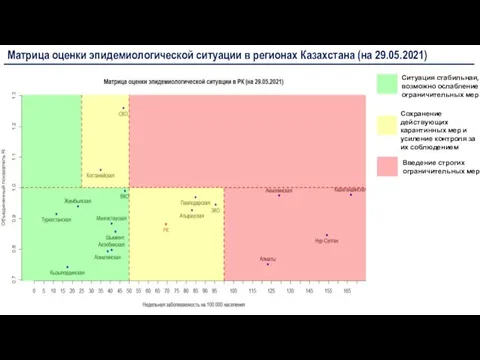 Матрица оценки эпидемиологической ситуации в регионах Казахстана
Матрица оценки эпидемиологической ситуации в регионах Казахстана Bacillus Major Reference Works
Bacillus Major Reference Works Фармацевтический рынок Украины. Что год грядущий нам готовит?.. Добранчук О.Л. Руководитель аналитической службы компании МОРИОН
Фармацевтический рынок Украины. Что год грядущий нам готовит?.. Добранчук О.Л. Руководитель аналитической службы компании МОРИОН  Физиологическое и психологическое развитие подростка
Физиологическое и психологическое развитие подростка Патологические переломы. Этиопатогенетическое лечение
Патологические переломы. Этиопатогенетическое лечение Игра. Средства, влияющие на функцию мочевыделительной системы
Игра. Средства, влияющие на функцию мочевыделительной системы Тыныс алу ағзалар ауруларының диагностикасындағы ЭКГ
Тыныс алу ағзалар ауруларының диагностикасындағы ЭКГ Количественные нарушения со стороны лейкоцитов
Количественные нарушения со стороны лейкоцитов Юкстагломерулярный аппарат почки
Юкстагломерулярный аппарат почки Трансаминирование. Тема 13
Трансаминирование. Тема 13 Бронхиальная астма
Бронхиальная астма СРС. Алгоритмы диагностики анемий и изменения гемостаза
СРС. Алгоритмы диагностики анемий и изменения гемостаза Раны, способы остановки кровотечений
Раны, способы остановки кровотечений lektsia_NMILS_FDPO_1_marta_2017
lektsia_NMILS_FDPO_1_marta_2017 Диспансеризация населения
Диспансеризация населения ВИЧ в Удмуртии: развитие эпидемии и современное состояние
ВИЧ в Удмуртии: развитие эпидемии и современное состояние Обследование больных с травмами и заболеваниями опорно-двигательного аппарата
Обследование больных с травмами и заболеваниями опорно-двигательного аппарата