Содержание
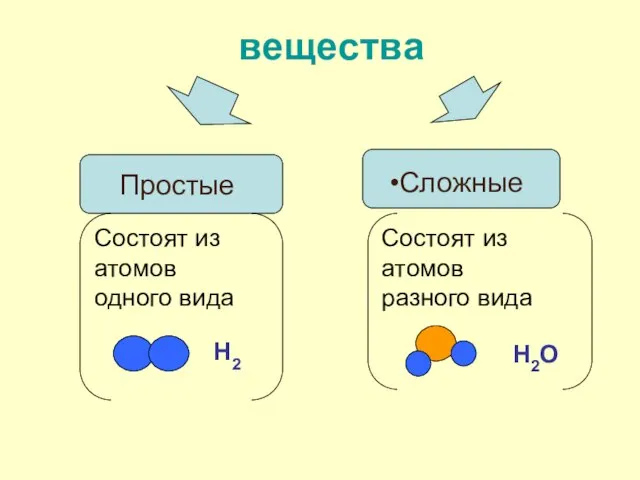
- 2. Сложные вещества Простые Состоят из атомов одного вида Состоят из атомов разного вида Н2 Н2О
- 3. Простые вещества
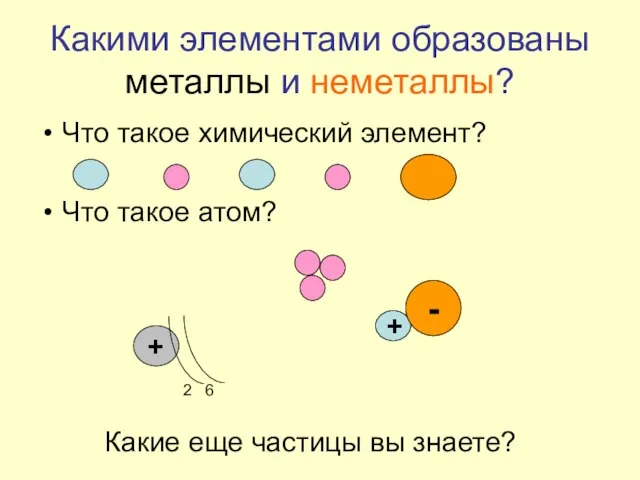
- 4. Какими элементами образованы металлы и неметаллы? Что такое химический элемент? Что такое атом? + 2 6
- 5. Сколько и каких частиц необходимо для образования: Молекулы кислорода Молекулы озона Молекулы воды Как отмерить нужное
- 6. Количество вещества Задачи урока: 1. Выяснить, что такое число Авогадро 2. Выяснить, что такое «моль», «молярная
- 7. Количество вещества m(C) = 12г NA = 6 ∙ 1023 – число Авогадро 1Моль - 6
- 8. Количество вещества Укажите количество (N) и вид частиц в: ∙ 1 моль алюминия (Al) 1 моль
- 9. Молярная масса М - [г/моль] М = m/n, n=m/M M = {Mr} г/моль
- 10. Количество вещества Моль – это …. Число Авогадро – это …. Молярная масса – это…. Молярная
- 12. Скачать презентацию




![Молярная масса М - [г/моль] М = m/n, n=m/M M = {Mr} г/моль](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/483154/slide-8.jpg)

 Алмашу реакциясе
Алмашу реакциясе Материальный и тепловой балансы абсорбции
Материальный и тепловой балансы абсорбции Понятия и законы в химии. (Лекция 1)
Понятия и законы в химии. (Лекция 1) Основные сведения о строении атома. Состав атомных ядер
Основные сведения о строении атома. Состав атомных ядер Основные понятия химической термодинамики
Основные понятия химической термодинамики Презентация на тему Теория строения органических соединений
Презентация на тему Теория строения органических соединений  Конкурс О, химия – ты муза вдохновения!
Конкурс О, химия – ты муза вдохновения! Алканы, предельные, насыщенные углеводороды (парафины)
Алканы, предельные, насыщенные углеводороды (парафины) Дисперсные системы
Дисперсные системы Важнейшие соединения хлора
Важнейшие соединения хлора Биогенный элемент. Кобальт (Со)
Биогенный элемент. Кобальт (Со) Характеристика металлов по положению в ПСХ
Характеристика металлов по положению в ПСХ Знаки химических элементов
Знаки химических элементов Диеновые углеводороды
Диеновые углеводороды Азотная кислота
Азотная кислота алотропні модифікації неметалів
алотропні модифікації неметалів Органическая химия как наука. Основные положения теории строения химических соединений. Структурная изомерия
Органическая химия как наука. Основные положения теории строения химических соединений. Структурная изомерия Свойства кремниевой кислоты и области применения силикатов
Свойства кремниевой кислоты и области применения силикатов Потенциометрический анализ, титрование
Потенциометрический анализ, титрование Алкены
Алкены Нефть и газ
Нефть и газ Исследование методов синтеза 5-аминосалициловой кислоты
Исследование методов синтеза 5-аминосалициловой кислоты Алкены.Номенклатура
Алкены.Номенклатура Презентация по Химии "Химическая номенклатура и филология"
Презентация по Химии "Химическая номенклатура и филология"  Аллотропия углерода
Аллотропия углерода Алюминий. Положение алюминия в периодической системе и строение его атома
Алюминий. Положение алюминия в периодической системе и строение его атома Бутан как хладагент
Бутан как хладагент Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу
Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу