Содержание
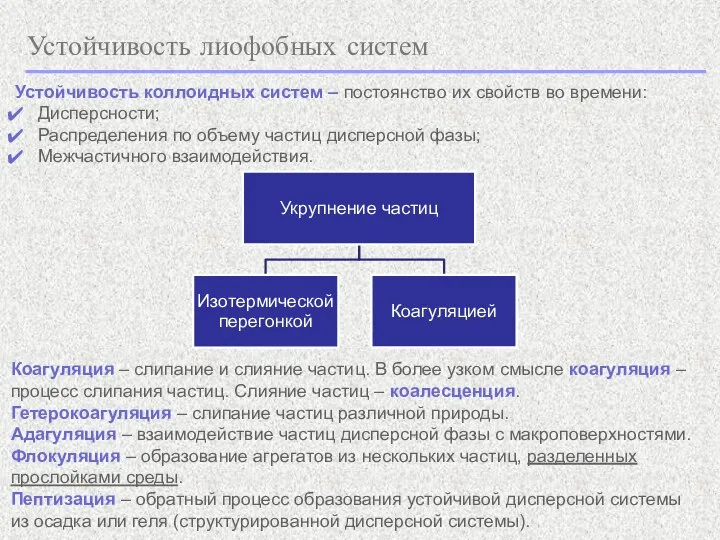
- 2. Устойчивость лиофобных систем Устойчивость коллоидных систем – постоянство их свойств во времени: Дисперсности; Распределения по объему
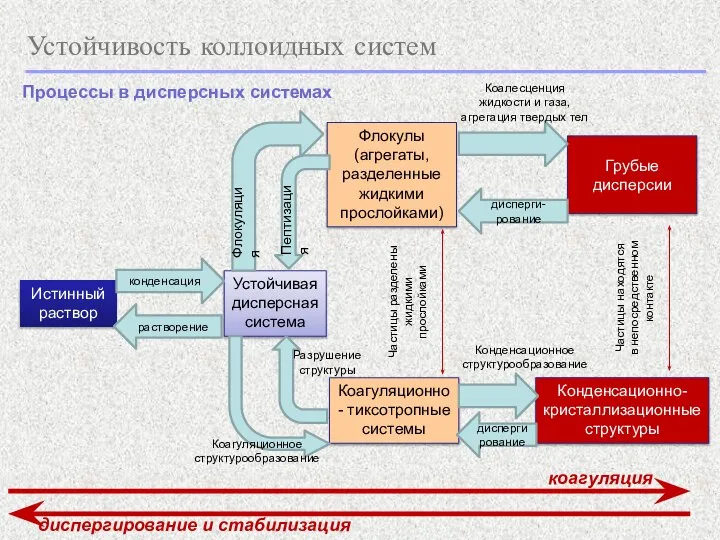
- 3. Процессы в дисперсных системах Истинный раствор Устойчивая дисперсная система Флокулы (агрегаты, разделенные жидкими прослойками) Коагуляционно- тиксотропные
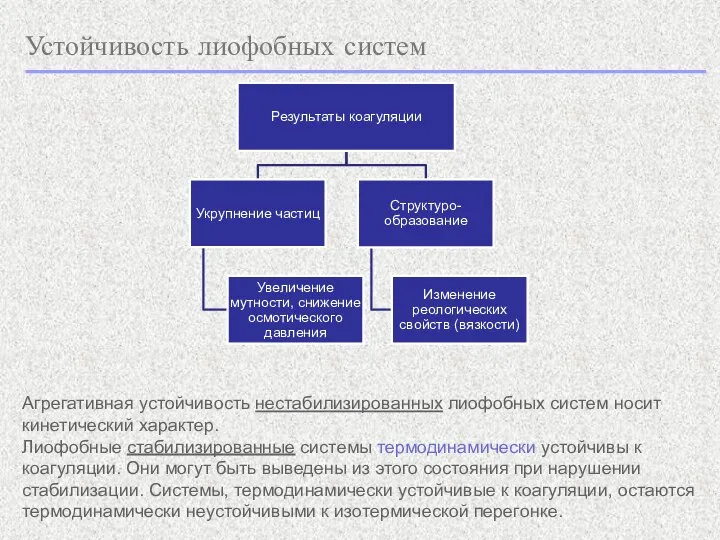
- 4. Устойчивость лиофобных систем Агрегативная устойчивость нестабилизированных лиофобных систем носит кинетический характер. Лиофобные стабилизированные системы термодинамически устойчивы
- 5. Изотермическая перегонка Зависимость растворимости от размера частиц: Изотермическая перегонка – процесс переноса вещества от мелких частиц
- 6. Изотермическая перегонка Имеют высокую энергию активации; Энергия активации для твердых частиц выше, чем для жидких
- 7. Изотермическая перегонка
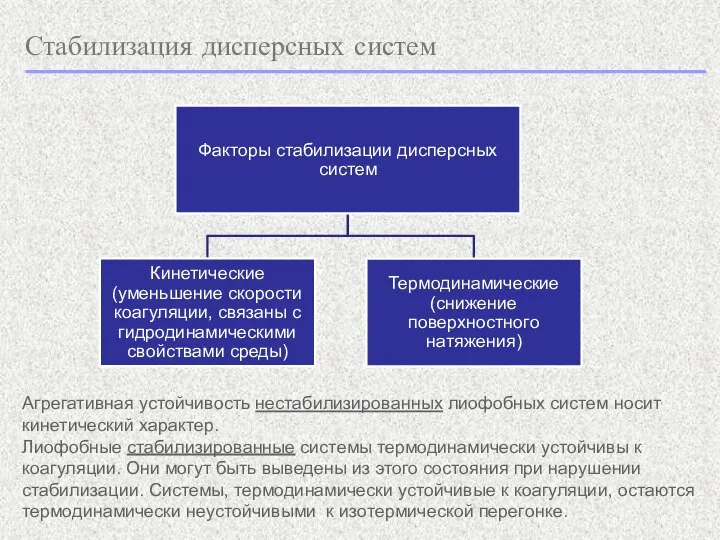
- 8. Стабилизация дисперсных систем Агрегативная устойчивость нестабилизированных лиофобных систем носит кинетический характер. Лиофобные стабилизированные системы термодинамически устойчивы
- 9. Факторы стабилизации дисперсных систем
- 10. Факторы стабилизации дисперсных систем В реальных системах часто действует комбинация различных факторов. Термодинамические факторы уменьшают вероятность
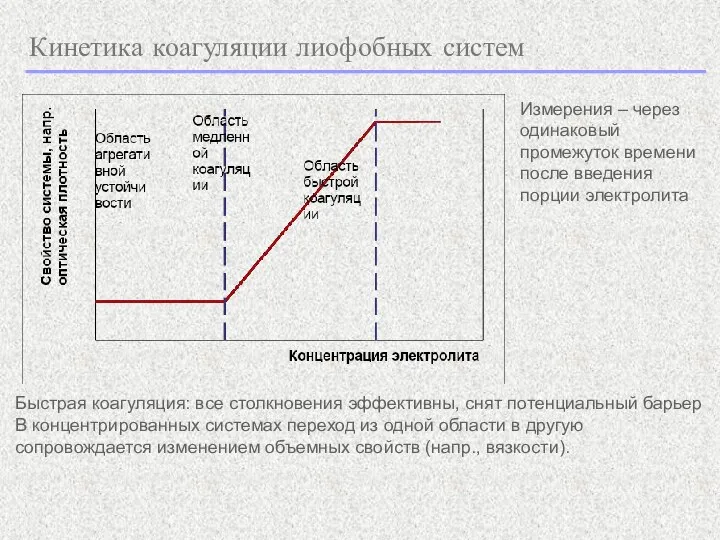
- 11. Кинетика коагуляции лиофобных систем Измерения – через одинаковый промежуток времени после введения порции электролита Быстрая коагуляция:
- 12. Кинетика коагуляции лиофобных систем r x Rп
- 13. Кинетика коагуляции лиофобных систем - уравнение Смолуховского
- 14. Кинетика коагуляции лиофобных систем 1
- 15. Кинетика коагуляции лиофобных систем
- 16. Кинетика коагуляции лиофобных систем
- 17. Кинетика коагуляции лиофобных систем
- 18. Кинетика коагуляции лиофобных систем Теория Мюллера Усовершенствование теории Мюллера: рассматриваются полидисперсные коллоидные системы. Основные выводы: Полидисперсные
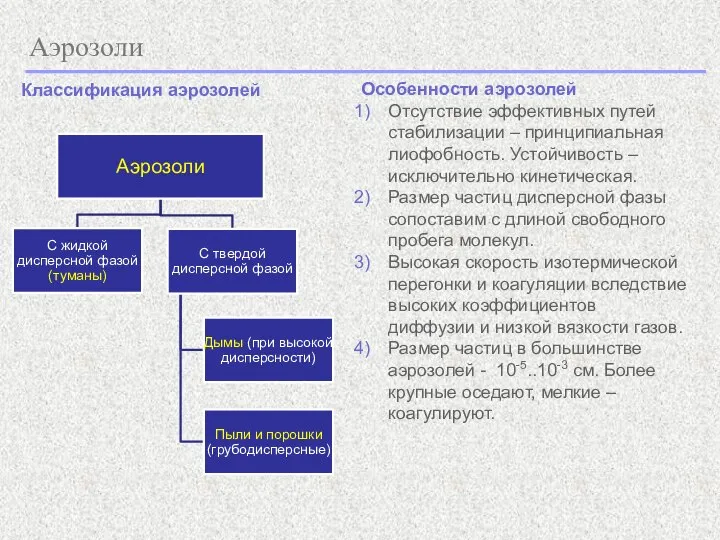
- 19. Аэрозоли Классификация аэрозолей Особенности аэрозолей Отсутствие эффективных путей стабилизации – принципиальная лиофобность. Устойчивость – исключительно кинетическая.
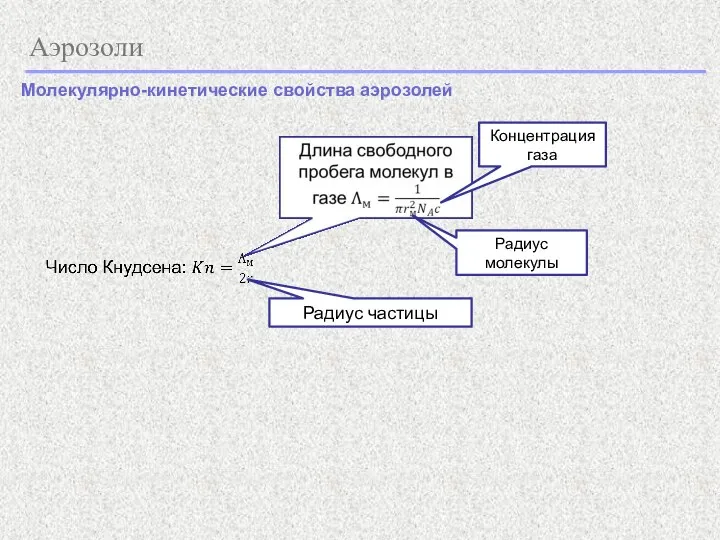
- 20. Аэрозоли Молекулярно-кинетические свойства аэрозолей Радиус частицы Радиус молекулы Концентрация газа
- 21. Аэрозоли Молекулярно-кинетические свойства аэрозолей
- 22. Аэрозоли Электрические свойства аэрозолей
- 23. Аэрозоли Применение аэрозолей Постановка дымовых завес; Применение отравляющих веществ; Применение ядохимикатов; Аэрозольные лекарственные формы; Бытовая химия;
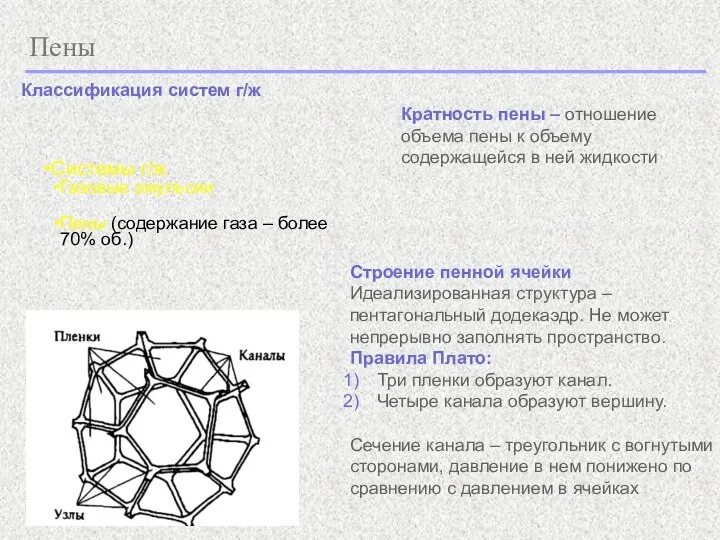
- 24. Пены Классификация систем г/ж Системы г/ж Газовые эмульсии Пены (содержание газа – более 70% об.) Строение
- 26. Скачать презентацию















 Углеводороды. Характеристика
Углеводороды. Характеристика Химическое равновесие
Химическое равновесие Электролитическая диссоциация
Электролитическая диссоциация Свойства кислот, оснований и солей как электролитов
Свойства кислот, оснований и солей как электролитов Аммиак. Состав. Строение. Химическая ковалентная полярная связь. Кристаллическая молекулярная решетка
Аммиак. Состав. Строение. Химическая ковалентная полярная связь. Кристаллическая молекулярная решетка Значимые личности в химии
Значимые личности в химии Презентация на тему История каучука
Презентация на тему История каучука  Способы защиты химического оборудования от коррозии
Способы защиты химического оборудования от коррозии Характеристика металлов по положению в ПСХ
Характеристика металлов по положению в ПСХ Предмет органической химии. Органические вещества
Предмет органической химии. Органические вещества Химическая связь в органических соединениях
Химическая связь в органических соединениях Углерод
Углерод Ароматические углеводороды
Ароматические углеводороды Согласованное и несогласованное действие заместителей в бензольном кольце
Согласованное и несогласованное действие заместителей в бензольном кольце Реакции ионного обмена. Задания. 9 класс
Реакции ионного обмена. Задания. 9 класс Презентация на тему А.М. Бутлерова
Презентация на тему А.М. Бутлерова  Показатель активности водородных ионов. Лабораторная работа №4
Показатель активности водородных ионов. Лабораторная работа №4 Тема урока: «Серная кислота» 9 класс
Тема урока: «Серная кислота» 9 класс Классификация органических соединений. Урок химии в 10 классе
Классификация органических соединений. Урок химии в 10 классе ТЭЦ, работающие на каменном угле более экологичны, чем на буром. Факт или вымысел?
ТЭЦ, работающие на каменном угле более экологичны, чем на буром. Факт или вымысел? Полимеры
Полимеры Теория строения химических соединений
Теория строения химических соединений Белки
Белки Иттрий-алюминиевый гранат и иттрий-алюминиевый перовскит
Иттрий-алюминиевый гранат и иттрий-алюминиевый перовскит Алкины
Алкины Применение обратимых и необратимых реакций в быту
Применение обратимых и необратимых реакций в быту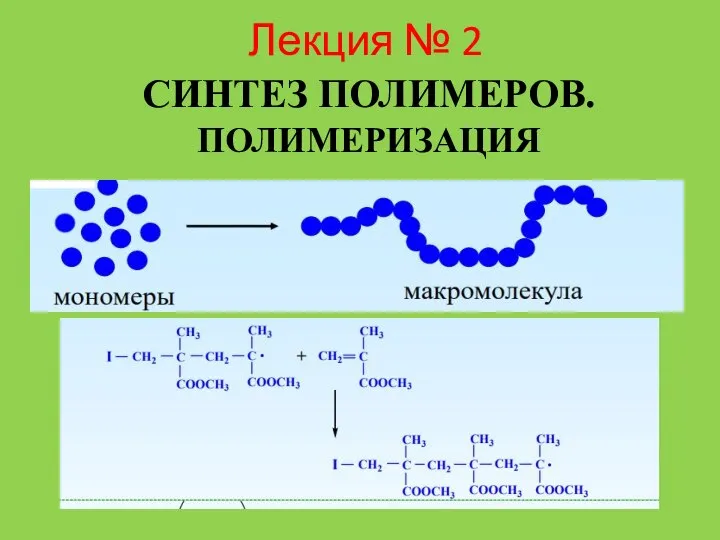 Лекция № 2. Синтез полимеров. Полимеризация
Лекция № 2. Синтез полимеров. Полимеризация Типы химических реакций
Типы химических реакций