Содержание
- 2. Реакции разложения
- 3. Реакции разложения - это такие реакции, в результате которых из одного сложного вещества образуется несколько новых
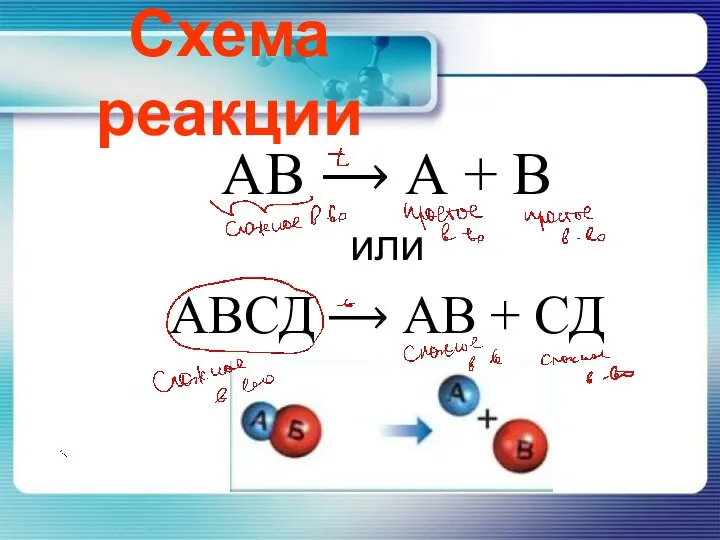
- 4. Схема реакции АВ ⟶ А + В или АВСД ⟶ АВ + СД
- 6. Типовые реакции разложения 1) Все нерастворимые основания разлагаются под действием t֯, с образованием оксида металла этой
- 7. 2) Нерастворимые кислородосодержащие соли разлагаются под действием t֯, с образованием оксида металла этой же валентности и
- 8. 3)Нерастворимая кислородосодержащая кислота (H2SiO3) разлагаются под действием t֯, с образованием оксида неметалла этой же валентности и
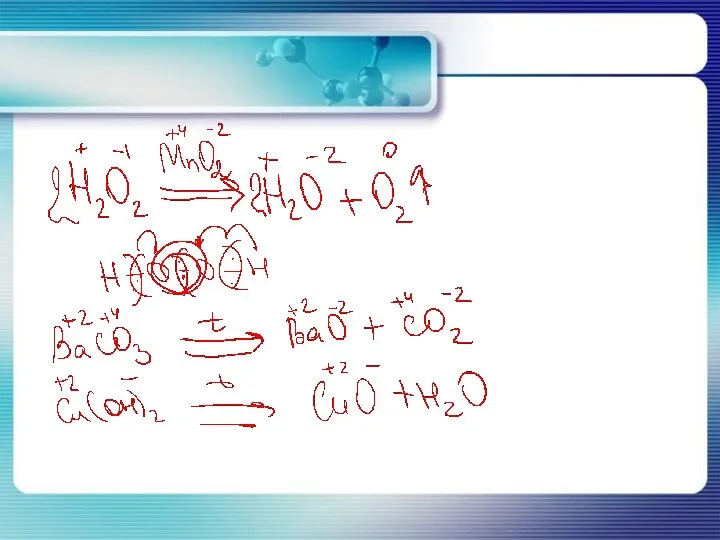
- 9. Типовые реакции разложения KMnO4 → K2MnO4 + MnO2 + O2↑ HNO3 → NO2↑ + O2↑ +
- 10. Основные понятия Катализаторы – это вещества, изменяющие скорость химической реакции, но по окончании их остающиеся качественно
- 12. Скачать презентацию







 Альдегиды. Номенклатура, изомерия. Получение альдегидов
Альдегиды. Номенклатура, изомерия. Получение альдегидов Относительная молекулярная масса
Относительная молекулярная масса Основные виды сырья для промышленности органического и нефтехимического синтеза
Основные виды сырья для промышленности органического и нефтехимического синтеза Обобщающий урок по теме «Соединения химических элементов» 8 класс.
Обобщающий урок по теме «Соединения химических элементов» 8 класс. Схема реакций
Схема реакций Технология производства пленок. Свойства полимерных пленочных материалов, модификация, применение
Технология производства пленок. Свойства полимерных пленочных материалов, модификация, применение Белки
Белки Реакции ионного обмена. Электролитическая диссоциация
Реакции ионного обмена. Электролитическая диссоциация Триады, октавы, спираль, таблица
Триады, октавы, спираль, таблица Сложные эфиры. Жиры
Сложные эфиры. Жиры Олеиновая кислота
Олеиновая кислота Элементы и атомы, В менделеевский взяты круг Сделали химию самой богатой И самой творческой из наук.
Элементы и атомы, В менделеевский взяты круг Сделали химию самой богатой И самой творческой из наук. Презентация на тему Вычисления массовой доли растворенного вещества
Презентация на тему Вычисления массовой доли растворенного вещества  Презентация на тему Органическая химия. История развития
Презентация на тему Органическая химия. История развития  Коррозия металлов (9 класс)
Коррозия металлов (9 класс) Виведення плям органічного походження
Виведення плям органічного походження Элемент первой группы, калий
Элемент первой группы, калий Презентация на тему Химическое равновесие
Презентация на тему Химическое равновесие  Сталь 12Х18Н10Т
Сталь 12Х18Н10Т Презентация на тему Аммиак
Презентация на тему Аммиак  ОГЭ химия. Основной государственный экзамен
ОГЭ химия. Основной государственный экзамен Флотационный способ обогащения
Флотационный способ обогащения Определение содержания солей в воде
Определение содержания солей в воде Презентация на тему Подготовка к ЕГЭ. Полезно знать
Презентация на тему Подготовка к ЕГЭ. Полезно знать  Пластификация пластмасс
Пластификация пластмасс Презентация на тему Растворы
Презентация на тему Растворы  Абсорбционная осушка газа
Абсорбционная осушка газа Презентация на тему Соединения серы
Презентация на тему Соединения серы